学外申請者の場合
※研究相談および手順確認をご希望ならヘルスサイエンスR&Dセンターまでお問合せください。 |
学内申請者の場合
|

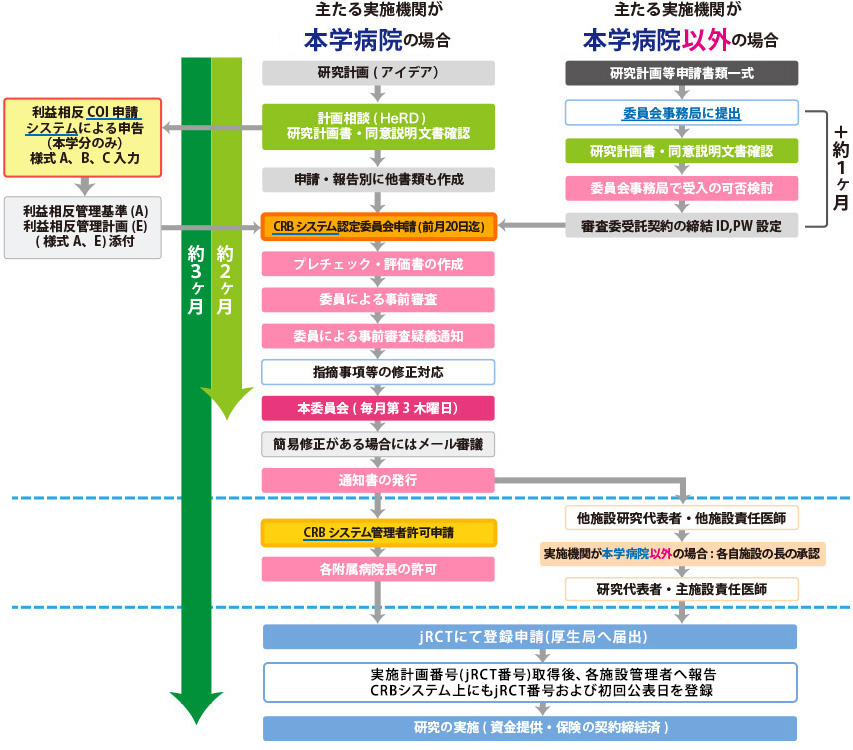
臨床研究法該当研究の申請の流れ
(A) 認定臨床研究審査委員会申請の流れ(B) 実施施設の管理者許可取得の流れ
(C) 必要な情報をjRCT上に入力、審査結果通知書を添付し、申請。
 |
 |
 |
|
 |

(CRBシステムに入力·添付)
| 新規申請 |
・新規審査依頼書(統一書式2)(CRBシステムでは省略) ・実施計画(様式第一) *jRCT入力で作成 ・研究計画書 ・説明文書、同意文書 *jRCT添付 ・研究分担医師リスト(統一書式1) ・疾病等が発生した場合の対応に対する手順書 ・モニタリングに関する手順書 ・利益相反管理基準(様式A) ・利益相反管理計画(様式E) ・医薬品等の概要を記載した書類(添付文書) ・監査に関する手順書 **緑字様式作成時は提出 ・統計解析計画書 ・効果安全性評価委員会の審議に関する手順書 ・症例報告書の見本 @審査結果通知書入手後、管理者から実施許可通知書受領、jRCTにて届出 |
| 変更申請 |
・変更申請書(統一書式3)(CRBシステムでは省略) ・実施計画事項変更届書(様式第二) *jRCT添付 ・変更した実施計画 *jRCT入力(実施計画書内容に変更ない場合は不要) ・各申請後変更のあった書類 @審査結果通知書入手後、管理者から実施許可通知書受領、jRCTにて届出 |
| 軽微変更 |
・軽微変更通知書(統一書式14)(CRBシステムでは省略) ・実施計画事項軽微変更届書(様式第三) ・変更部分複写 (担当氏名のみ変更、地域名称の変更など) @jRCT上で届出後、10日以内に委員会に報告 |
| 定期報告 |
| 疾病等報告 |
(医薬品・医療機器・再生医療等
・医薬品疾病等報告書(第 報)(統一書式8)製品別に様式が異なる) ・疾病等報告書(医薬品:別紙様式2-1) ・医療機器疾病等又は不具合報告書 (統一書式9) ・疾病等報告書(医療機器:別紙様式2-2) ・再生医療等製品疾病等又は不具合報告書(統一書式10) @jRCTシステムで報告(7日、15日、30日以内) @定期報告時にも委員会に報告し、管理者に報告 |
重大な不適合報告 |
・重大な不適合報告書(統一書式7) @管理者に報告 |
その他報告 |
・その他の報告(管理者報告で重大でない不適合報告、重大でない疾病、jRCT番号報告等) @管理者に報告 |
| 中止届 | ・中止通知書(統一書式11) ・特定臨床研究中止届(様式第四) @10日以内に委員会に通知 @1年以内に総括報告書(の概要)作成し提出 |
| 終了通知 | ・主要評価項目報告書(概要)(総括報告書と同時期なら不要) @主評価項目データ収集終了後1年以内に、変更申請の手続きで提出 ・総括報告書 ・終了通知書(統一書式12) ・終了届書(=総括報告書の概要) (別紙様式1) @全データ収集終了後1年以内に委員会に提出 @委員会審査結果通知書受領後、終了届書に研究計画書、統計解析計画書(作成した場合)を添付し、1ヵ月以内にjRCTにて届出 |
・厚生労働大臣に提出必要な書類(特定のみ)
**作成した場合添付
【本学申請者の場合】審査結果通知書入手後、CRBシステムにて審査結果通知書添付し管理者の実施許可申請
| 統一書式 | 資料名 | ダウンロード |
|---|---|---|
| 書式1 | 研究分担医師リスト | 厚生労働省HP |
| 書式2 | 新規審査依頼書 | |
| 書式3 | 変更審査依頼書 | |
| 書式4 | 審査結果通知書 | |
| 書式5 | 定期報告書 | |
| 書式6 | 軽微変更通知書 | |
| 書式7 | 重大な不適合報告書 | |
| 書式8 | 医薬品の疾病等報告書 | |
| 書式9 | 医療機器の疾病等又は不具合報告書 | |
| 書式10 | 再生医療等製品の疾病等又は不具合報告書 | |
| 書式11 | 中止通知書 | |
| 書式12 | 終了通知書 | |
| 書式13 | 認定臨床研究審査委員会の意見報告書 | |
| 詳細記載用書式 | 書式8~10の詳細記載用 | |
| 参考書式1 | 技術専門員評価書 | |
| 参考書式2 | 実施医療機関の要件 | |
| 参考書式3 | 技術専門員就任依頼書 | |
| 参考書式4 | 履歴書 | |
| 参考書式5 | 適応外使用該当性確認依頼書 | |
| 参考書式6 | 適応外使用該当性評価書 |
| 省令様式 | 資料名 | |
|---|---|---|
| 様式第一(39条関係) | 実施計画 | jRCT上で作成・提出 |
| 様式第二(41条関係) | 実施計画変更届書 | |
| 様式第三(43条関係) | 実施計画軽微変更届書 | |
| 様式第四(45条関係) | 特定臨床研究中止届書 |
| 施行通知 別紙様式 | 資料名 | |
|---|---|---|
| 別紙様式1 | 終了届書 | jRCT上で作成・提出 |
| 別紙様式2-1 | 疾病等報告書(医薬品) | |
| 別紙様式2-2 | 疾病等報告書(医療機器) | |
| 別紙様式3 | 定期報告書 |
| (本学)特定様式2 | jRCT登録報告書 |